Wirkstoffforschung
- Zell- und Tumorbiologie

Dr. Aubry Miller
Group Leader

Dr. Peter Nikolas Gunkel
Group Leader
Die Übertragung neuer Erkenntnisse aus der Krebsforschung in neuartige Therapeutika ist ein grundlegender Schritt auf dem Weg zu einem Leben ohne Krebs. Die Arbeitsgruppe Wirkstoffforschung macht den ersten Schritt auf diesem Weg: die Entdeckung und Entwicklung kleinmolekularer Substanzen, die präzise darauf abgestimmt sind, spezifische onkogene Proteine zu hemmen und individuelle Kennzeichen von Krebs gezielt zu adressieren.
Unsere Forschung

Wir nutzen und teilen maßgeschneiderte kleinmolekulare Sonden als Forschungswerkzeuge, um unbeantwortete biologische Fragen zu adressieren (z. B. DKFZ-748). Darüber hinaus entwickeln wir unsere Inhibitoren zu Leitstrukturen für nachfolgende Arzneimittelentwicklungsprojekte weiter (z. B. DKFZ-682). Die Forschung in unserer Gruppe umfasst die Identifikation und Validierung von Zielstrukturen, die Entwicklung von Assays für Screening-Kampagnen, die chemische Synthese zur Optimierung von Trefferstrukturen und Sonden sowie die Etablierung zellbasierter Assays zur Bewertung der Wirksamkeit und Wirkmechanismen unserer Inhibitoren.
Das ideale Ergebnis unserer Projekte ist ein Wirksamkeitsnachweis in Tiermodellen, der die Grundlage für Entwicklungsinitiativen bildet, die durch öffentliche und private Fördermittel unterstützt werden. Mit umfassender Expertise in den strategischen und technischen Aspekten der Arzneimittelforschung ist unser Team zielklassenagnostisch und arbeitet regelmäßig mit DKFZ-Kollegen zusammen, die ihre Forschungsergebnisse in kleinmolekulare Inhibitoren oder Therapeutika übersetzen möchten.
Projekte
Ein wichtiger Grund für den begrenzten Erfolg echter Redox-targeting Medikamente in der Klinik ist das Fehlen eines Biomarker-Konzepts, das dabei hilft, jene Krebspatienten zu identifizieren, die am wahrscheinlichsten auf ROS-induzierende Medikamente ansprechen. Mithilfe von Proteomik-, Transkriptomik- und Medikamentensensitivitätsdaten aus einer großen Panel-Analyse von Adenokarzinom-Zelllinien des nicht-kleinzelligen Lungenkrebses identifizierten wir eine Gruppe von 15 Biomarkern, die die Wirksamkeit von Medikamenten – sowohl unserer TXNRD1-Inhibitoren als auch verwandter Wirkstoffe wie Ferroptose-Induktoren – präzise vorhersagen [Samarin et al. 2023]. Diese Gruppe, die wir als Anti-Oxidant Capacity Biomarkers (ACBs) bezeichnen, umfasst zentrale Signalwege der Redoxregulation und des Schutzes vor oxidativem Stress und ist in empfindlichen Zellen stark reprimiert. Entgegen der Erwartungen ist die konstitutiv niedrige ACB-Expression nicht mit erhöhten basalen Spiegeln reaktiver Sauerstoffspezies (ROS) verbunden, sondern mit einem hohen Gehalt an Stickstoffmonoxid, das notwendig ist, um hohe Replikationsraten aufrechtzuerhalten. ACBs sind nur bei einer kleinen Untergruppe von Patienten in den meisten Krebsarten günstig exprimiert, mit dem höchsten Anteil bei Leukämien und kleinzelligem Lungenkrebs (SCLC). In resistenten Zellen sind ACBs aufgrund von Mutationen im negativen Regulator von NRF2, KEAP1, stark exprimiert. Überraschenderweise führte die pharmakologische Hemmung von KEAP1 weder zu einer erhöhten Resistenz von Krebszellen gegenüber Chemotherapeutika noch gegenüber Ferroptose- oder Redox-targeting Medikamenten. Im Gegensatz dazu reagieren Zellen aus normalem Gewebe auf eine pharmakologische NRF2-Induktion mit einer Hochregulierung von ROS-abbauenden Enzymen und überstehen medikamenteninduzierte Apoptose länger. Diese Beobachtung spiegelt sich vollständig in Mausmodellen für therapiebedingte Organschäden wider, die zeigen, dass die pharmakologische Induktion von NRF2 dosislimitierende Nebenwirkungen abschwächt. Derzeit untersuchen wir, ob die differenzielle Regulation von ACBs in Tumorgewebe im Vergleich zu gesundem Gewebe genutzt werden kann, um das therapeutische Fenster von Redox-targeting Medikamenten zu erweitern.
Histondeacetylasen (HDACs) sind eine Gruppe von Hydrolase-Enzymen, die für die Entfernung von Acylgruppen, hauptsächlich von Lysinresten auf Proteinen, aber auch von anderen acylierten Aminderivaten, verantwortlich sind. HDAC10 ist beispielsweise bekannt dafür, ein schwacher Lysindeacetylase, jedoch ein effizienter Deacetylase für Polyamine (z. B. Spermidin) zu sein. Darüber hinaus haben mehrere Studien HDAC10 als potenzielles Ziel für Krebsmedikamente hervorgehoben: (1) Hohe HDAC10-Expressionsniveaus korrelieren mit einer schlechten klinischen Prognose bei Patienten mit fortgeschrittenem Neuroblastom im Stadium 4, die eine Chemotherapie erhalten haben. (2) Konsistent mit diesen Befunden führt der Verlust von HDAC10 in Neuroblastomzellen zu einer Unterbrechung des autophagischen Flusses und sensibilisiert die Zellen für Chemotherapie, während die Überexpression von HDAC10 Neuroblastomzellen vor einer Behandlung mit Doxorubicin schützt.
Wir haben die ersten systematischen Untersuchungen zur Entwicklung von HDAC10-Inhibitoren veröffentlicht und festgestellt, dass eine Reihe vermeintlich selektiver HDAC6-Inhibitoren auch sehr gute HDAC10-Inhibitoren sind. Tatsächlich haben wir gezeigt, dass Tubastatin A, einer der bekanntesten HDAC6-Inhibitoren, ein noch besserer HDAC10-Binder ist. Kürzlich haben wir die ersten vollständig charakterisierten, hochselektiven chemischen Sonden für HDAC10 veröffentlicht. Derzeit konzentriert sich unsere Arbeit auf die Synthese von HDAC10-PROTACs und die Verwendung dieser Verbindungen, um die HDAC10-Biologie und sein Potenzial als therapeutisches Ziel in der Krebstherapie besser zu verstehen.
Kallikrein-related Peptidasen (KLKs) sind eine Familie von 15 sekretorischen Serinproteasen, die in einer Vielzahl pathologischer Zustände eine Rolle spielen. Während KLKs hauptsächlich als Biomarker untersucht wurden, wird zunehmend deutlich, dass sie auch direkt an der Krankheitsprogression beteiligt sind. KLK6 beispielsweise fördert die Migration und Invasion von Tumorzellen bei Melanomen und Darmkrebs, doch in der Literatur gibt es bisher nur wenige Berichte über KLK6-Inhibitoren.
Wir haben kürzlich eine neuartige Serie von Depsipeptiden beschrieben, die kovalente Inhibitoren von KLK6 darstellen. Nach einer gründlichen Untersuchung der Struktur-Wirkungs-Beziehungen (SAR) und des Wirkmechanismus (MOA) dieser Substanzen haben wir sie durch die Einführung eines Alkin-Handgriffs in Aktivitätssonden umgewandelt. Diese Sonden können verwendet werden, um endogenes KLK6 aus Zelllinien zu isolieren und eine erste Schätzung der enzymatischen Aktivität in biologischen Proben zu ermöglichen.
Derzeitige Arbeiten zielen darauf ab, diese Inhibitoren/Sonden weiter zu verbessern und eine zuverlässige diagnostische Methode zur Messung der KLK6-Aktivität in humanen Proben zu entwickeln.
Wir haben in den letzten zehn Jahren umfassende Expertise in der Synthese und Charakterisierung bifunktionaler Degrader (z. B. PROTACs) aufgebaut. Derzeit arbeiten wir an vier verschiedenen Degrader-Projekten, einschließlich HDAC10-PROTACs, doch diese Projekte wurden bisher noch nicht veröffentlicht
Team
Unser Team ist eine interdisziplinäre Gruppe aus Zellbiologen, Biochemikern und synthetischen organischen Chemikern, die gemeinsam daran arbeiten, neue kleinmolekulare Inhibitoren und Arzneimittelleitstrukturen zu entdecken und zu entwickeln.
- Profil anzeigen

Dr. Aubry Miller
Group Leader
-

Dr. Peter Nikolas Gunkel
Group Leader
-

Nicole de Vries
Technician
-

Franziska Deis
Technician
-

Laura Ebert
Master's Student
-

Julia Hütt
Bachelor's student
-
Dr. Roman Kurilov
Bioinformatician
-

Dr. Hana Nuskova
Postdoc
-

Luka Obradovic
PhD Student
-
Hannelore Pink
Technician
-

Dr. Heiko Rebmann
Postdoc
-

Lisa Renz
- Profil anzeigen

Nick Richert
PhD Student
-

Jasmin Rogalski
Technician
-

Dr. Jana Samarin
Postdoc
- Profil anzeigen

Dr. Moritz Spiske
Postdoc
-

Anuar Utebayev
Bachelor's student
Ausgewählte Publikationen
T. Marker, R.R. Steimbach, C. Perez-Borrajero, M. Luzarowski, E. Hartmann, S. Schliech, D. Pastor-Flores, E. Espinet, A. Trumpp, A.A. Teleman, F. Gräter, B. Simon, A.K. Miller*, T.P. Dick* (* = co-corresponding authors)
J. Samarin, H. Nůsková, P. Fabrowski, M. Malz, E. Amtmann, M.J. Taeubert, D. Pastor-Flores, D. Kazdal, R. Kurilov, N. de Vries, H. Pink, F. Deis, J. Hummel-Eisenbeiss, K. Kaushal, T.P. Dick, G. Hamilton, M. Muckenthaler, M. Mall, B. Lim, T. Kanamaru, G. Klinke, M. Sos, J. Frede, A.K. Miller, H. Alborzinia, N. Gunkel
R.R. Steimbach, C.J. Herbst-Gervasoni, S. Lechner, T.M. Stewart, G. Klinke, J. Ridinger, M.N.E. Geraldy, G. Tihanyi, J.R. Foley, U. Uhrig, B. Küster, G. Poschet, R.A. Casero Jr., G. Medard, I. Oehme, D.W. Christianson, N. Gunkel, A.K. Miller
S. Jänner*, D. Isak*, Y. Li, K.N. Houk, A.K. Miller
M. Morgen, P. Fabrowki, E. Amtmann, N. Gunkel, A.K. Miller
Denksport
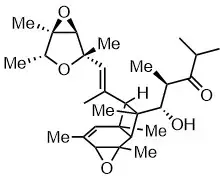
Unser Synthese (Denksport)-Klub trifft sich alle zwei Wochen, um Strategien und Mechanismen durch die Untersuchung aktueller oder klassischer Synthesen zu diskutieren. Bitte Aubry kontaktieren (siehe unten), wenn Sie Interesse haben, mitzumachen.
Die Denksportaufgaben finden Sie hier.
Kontaktieren Sie uns


