Wenn ausreichend Nährstoffe aus dem Blut zur Verfügung stehen, importieren die Zellen unseres Körpers als bevorzugtes Nahrungsmittel freie Aminosäuren, die Bausteine von Proteinen. Doch Tumoren sind oft unzureichend mit Blut versorgt, den Krebszellen stehen dann wenig Nährstoffe zur Verfügung. Darauf können sie mit Stoffwechselanpassungen reagieren und bei Hungerzuständen auf alternative Nährstoffquellen umschalten. Unter diesen Bedingungen nutzen sie insbesondere den Abbau von Proteinen aus ihrer Umgebung als Nahrungsquelle. Die Mechanismen, mit denen Krebszellen dies gelingt, sind jedoch nur unzureichend erforscht.
Um die molekularen Schritte, die dieser Stoffwechselanpassung zugrunde liegen, besser zu verstehen, haben sich Wissenschaftlerinnen und Wissenschaftler vom Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg und vom Forschungsinstitut für Molekulare Pathologie (IMP) in Wien zusammengetan. Das Team untersuchte Krebszellen unter streng kontrollierten Nährstoffbedingungen, die einen Aminosäuremangel imitierten, wie er in vielen Tumoren auftritt. Mit der „Genschere“ CRISPR-Cas9 schalteten die Forscher die Expression fast aller Gene im Erbgut einzeln aus. Auf diese Weise konnten sie die genetischen Komponenten der Signalwege identifizieren, die am Umschalten auf die neue Nährstoffquelle beteiligt sind.
Dabei entdeckte die Forscher ein bislang nicht charakterisiertes Gen, das ausschließlich dann für das Überleben erforderlich ist, wenn sich die Krebszellen von extrazellulären Proteinen ernähren. Das Gen stellt den Bauplan für das Membranprotein „LYSET“ (Lysosomal Enzyme Trafficking Factor), das sich als entscheidend für die Funktion der Lysosomen erwies. Diese kleinen Zellstrukturen dienen der Zelle als Magen und verdauen Proteine.
LYSET stellte sich als Kernkomponente des so genannten Mannose-6-Phosphat-Wegs heraus, der für die Befüllung der Lysosomen mit Verdauungsenzymen erforderlich ist. Fehlt LYSET, fehlen den Krebszellen die Enzyme in ihren Lysosomen und sie sind nicht mehr in der Lage, die Nährstoffquelle zu wechseln. Für das Wachstum von Tumoren hat das dramatische Auswirkungen: An Mäusen, bei denen Krebs ausgelöst wurde, konnten die Forscher zeigen, dass ein Verlust von LYSET die Tumorentwicklung stark verlangsamt.
Wilhelm Palm vom DKFZ sagt: “Mit LYSET haben wir eine zentrale Komponente eines Stoffwechselweges entdeckt, der den Krebszellen die Anpassungen an verschiedene Nährstoffe ermöglicht. Das ist ihre Schlüsselfähigkeit, um in einer kargen Tumorumgebung zu überleben und zu wachsen.“
„Das macht die Entdeckung so spannend“, sagt Johannes Zuber vom IMP. „LYSET und der Mannose-6-Phosphat-Stoffwechselweg erweisen sich als besonders wichtig für Krebszellen und könnten daher ein molekularer Ansatzpunkt sein, um einen wichtigen Stoffwechselengpass bei Krebs therapeutisch anzugreifen.“
Catarina Pechincha, Sven Groessl, Robert Kalis, Melanie de Almeida, Andrea Zanotti, Marten Wittmann, Martin Schneider, Rafael P. de Campos, Sarah Rieser, Marlene Brandstetter, Alexander Schleiffer, Karin Müller-Decker, Dominic Helm, Sabrina Jabs, David Haselbach, Marius K. Lemberg, Johannes Zuber, Wilhelm Palm: Lysosomal enzyme trafficking factor LYSET enables nutritional usage of extracellular proteins.
Science 2022, doi.org/10.1126/science.abn5637
Ein Bild zur Meldung steht zum Download zur Verfügung:
Illustration-dq-lysotracker.jpg
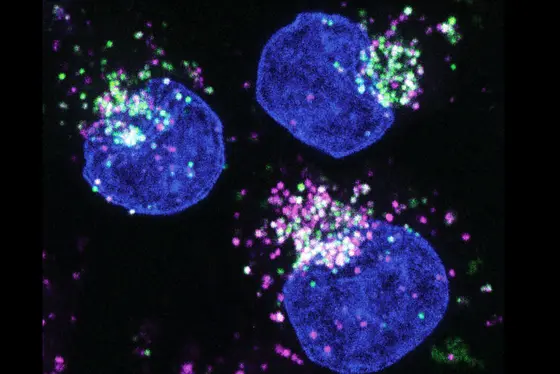
BU: Menschliche Krebszellen (blau: Zellkerne) nehmen extrazelluläre Proteine auf (Albumin, grün). Die Proteine werden in Lysosomen (pink) zu Aminosäuren verdaut, die dann als Nährstoffquelle genutzt werden.
Nutzungshinweis für Bildmaterial zu Pressemitteilungen
Die Nutzung ist kostenlos. Das Deutsche Krebsforschungszentrum (DKFZ) gestattet die einmalige Verwendung in Zusammenhang mit der Berichterstattung über das Thema der Pressemitteilung bzw. über das DKFZ allgemein. Bitte geben Sie als Bildnachweis an: „Quelle: W. Palm / DKFZ. Eine Weitergabe des Bildmaterials an Dritte ist nur nach vorheriger Rücksprache mit der DKFZ-Pressestelle (Tel. 06221 42 2854, E-Mail: presse@dkfz.de) gestattet. Eine Nutzung zu kommerziellen Zwecken ist untersagt.