Genau wie gesundes Gewebe sind Tumoren auf Nährstoffe angewiesen, die sie über den Blutkreislauf erhalten. Doch da Krebszellen sich rasch vermehren und die Geschwülste entsprechend schnell wachsen, kann hier ein Engpass entstehen – wenn nicht gleichzeitig auch neue Blutgefäße sprießen. Zudem stellen diese neuen Blutgefäße Transportwege dar, über die Krebszellen zu entfernten Organen gelangen, wo sie zu Metastasen auswachsen. Ein Ziel in der Krebstherapie ist es daher, die Angiogenese, also die Neubildung von Blutgefäßen zu unterbinden, um Tumoren so den Saft abzudrehen und so die Metastasierung zu verlangsamen. Entsprechende Wirkstoffe, die einen Signalweg der Angiogenese unterdrücken, sind bereits im klinischen Einsatz – allerdings mit begrenzter Wirkung.
Bereits vor zwei Jahren haben die Heidelberger und Mannheimer Forscher um Hellmut Augustin einen neuen Angriffspunkt entdeckt, über den das funktionieren könnte: Ein Rezeptormolekül namens Tie1. Es wird in den Endothelzellen gebildet, also in der Zellschicht, die die Blutgefäße von innen auskleidet. Bekannt ist außerdem, dass Tie1 bei der Tumorentwicklung und beim Wachstum von Blutgefäßen im Tumor vermehrt entsteht. „Wir kennen den Bindungspartner von Tie1 nicht und können daher noch nicht im Detail sagen, wie der Rezeptor wirkt“, sagt DKFZ Forscher Mahak Singhal, Erstautor der aktuellen Studie. Was die Wissenschaftler aber herausgefunden haben: Tie1 trägt bei fortschreitenden Krebserkrankungen dazu bei, dass sich das Wachstum der Blutgefäße und der Tumoren selbst beschleunigt. Außerdem destabilisiert Tie1 die Wände der Blutgefäße und fördert dadurch das Entstehen von Metastasen. Wird Tie1 bei Mäusen genetisch ausgeschaltet, unterdrückt dies sowohl das Tumorwachstum als auch die Metastasierung.
Tie1 ist demnach ein interessanter Angriffspunkt für die Krebstherapie. Vor diesem Hintergrund testeten die Wissenschaftler um Augustin eine Reihe von Antikörpern, die gegen Tie1 gerichtet sind. Tatsächlich konnten sie einen vielversprechenden Kandidaten ausmachen. Behandelten sie Mäuse, die Brust- oder Lungentumoren hatten, mit diesem Antikörper, so verlangsamte sich das Krebswachstum. Ein nennenswerter Effekt auf die Bildung von Blutgefäßen in den Tumoren ließ sich jedoch nicht beobachten. Dafür wiesen die behandelten Tiere signifikant weniger Metastasen auf als unbehandelte Mäuse mit Brust- oder Lungentumoren.
Das heißt, der Antikörper kann zwar die Angiogenese im Tumor nicht wirksam verhindern, birgt aber das Potenzial, bei einer Krebstherapie die Metastasenbildung auszubremsen. „Noch allerdings haben wir nur bei Versuchstieren beobachtet, dass der Antikörper eine therapeutische Wirkung hat“, betont Studienleiter Hellmut Augustin, dem es wichtig ist, keine verfrühten Hoffnungen zu wecken. „Bis er vielleicht tatsächlich eines Tages zur Behandlung von Krebspatienten zum Einsatz kommt, braucht es noch viele Experimente und Studien.“
Singhal M, Gengenbacher N, La Porta S, Gehrs S, Shi J, Kamiyama M, Bodenmiller DM, Fischl A, Schieb B, Besemfelder E, Chintharlapalli S, Augustin HG. Preclinical validation of a novel metastasis-inhibiting Tie1 function-blocking antibody. EMBO Molecular Medicine 2020, DOI: 10.15252/emmm.201911164
Ein Bild zur Pressemitteilung steht zur Verfügung unter:
Augustin_Lungenmetastasen_Maus_EMBO.jpg
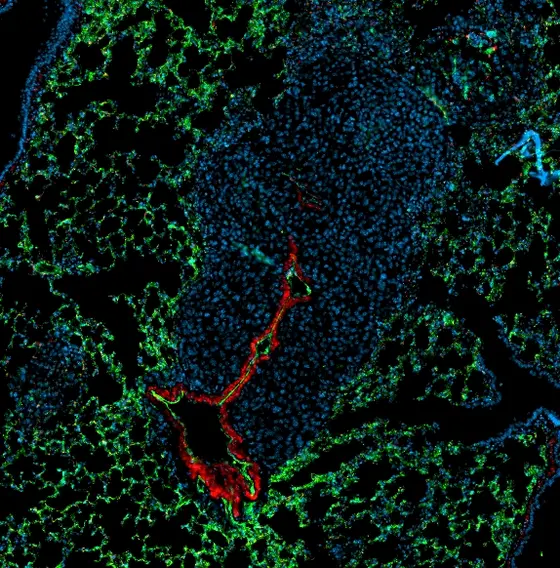
BU: Ein Blutgefäß (rot) wächst in die Metastase (blau) in der Lunge einer Maus ein.
Nutzungshinweis für Bildmaterial zu Pressemitteilungen
Die Nutzung ist kostenlos. Das Deutsche Krebsforschungszentrum (DKFZ) gestattet die einmalige Verwendung in Zusammenhang mit der Berichterstattung über das Thema der Pressemitteilung bzw. über das DKFZ allgemein. Als Bildnachweis ist folgendes anzugeben: „Quelle: Augustin/DKFZ“.
Eine Weitergabe des Bildmaterials an Dritte ist nur nach vorheriger Rücksprache mit der DKFZ-Pressestelle (Tel. 06221 42 2854, E-Mail: presse@dkfz.de) gestattet. Eine Nutzung zu kommerziellen Zwecken ist untersagt.