Bei Patienten mit akuter myeloischer Leukämie (AML) kommt es nach zunächst scheinbar erfolgreicher Behandlung häufig zu Rückfällen. Dafür mitverantwortlich sind Leukämie-Stammzellen, die die Therapie überlebt haben. Wissenschaftler können dies teilweise erklären: Die Stammzellen verfügen über Schutzmechanismen, die sie gegen Chemotherapie resistent machen. Doch wie gelingt es ihnen, auch der Immunabwehr zu entkommen?
Das hat nun ein Team aus Wissenschaftlern von der Universität und Universitätsklinik Basel, der Universitätsklinik Tübingen, vom Deutschen Krebsforschungszentrum (DKFZ), vom Heidelberg Institute for Stem Cell Technology and Experimental Medicine (HI-STEM)* und dem Deutschen Krebskonsortium (DKTK) untersucht und dabei einen überraschenden Mechanismus entdeckt.
Die Forscher analysierten Leukämiezellen von 177 AML-Patienten und fanden heraus: Die Krebsstammzellen unterdrücken auf ihrer Oberfläche die NKG2D-L Proteine. An diesen Eiweißstrukturen erkennen die zum Immunsystem zählenden natürlichen Killerzellen (NK-Zellen) normalerweise, ob eine Zelle beschädigt, infiziert oder zu Krebs mutiert ist und können sie dann gegebenenfalls abtöten. Durch das Fehlen von NKG2D-L entgehen die Leukämie-Stammzellen der Vernichtung durch das Immunsystem. Leukämie-Zellen ohne Stammzelleigenschaften dagegen präsentieren diese Zielmoleküle auf ihrer Oberfläche und werden daher von den NK-Zellen in Schach gehalten.
An Mäusen, denen AML-Zellen von Patienten übertragen worden waren, zeigten die Forscher: Während die normalen AML-Zellen (ohne Stammzelleigenschaften) von den NK-Zellen im Zaum gehalten wurden, entkamen die NKG2D-L-negativen Leukämie-Stammzellen dem Killerkommando. „Ein solcher Zusammenhang zwischen Stammzell-Eigenschaften und der Fähigkeit, dem Immunsystem zu entkommen, war bislang nicht bekannt“, sagt Claudia Lengerke vom Universitätsspital Basel und von der Universität Basel. „Ein wesentlicher Mechanismus dieser selektiven Immunresistenz in Stammzellen ist offenbar die Unterdrückung von Gefahrensignalen wie den NKG2D-L-Proteinen auf der Zelloberfläche“, ergänzt Helmut Salih vom Universitätsklinikum Tübingen und vom Deutschen Krebskonsortium (DKTK).
Was steckt hinter diesem außergewöhnlichen Schutzmechanismus? Den Wissenschaftlern fiel auf, dass die Leukämie-Stammzellen besonders viel PARP1 bilden, ein Enzym, das offenbar die NKG2D-L-Produktion blockiert. Dass PARP1 tatsächlich eine wichtige Rolle bei der Immunflucht spielt, zeigten abermals präklinische Versuche mit Mäusen, denen menschliche Leukämiezellen übertragen worden waren: Wurden diese Tiere mit Medikamenten behandelt, die PARP1 hemmen, bildeten die Leukämie-Stammzellen wieder NKG2D-L auf ihrer Oberfläche – und wurden daraufhin von ebenfalls transferierten menschlichen NK-Zellen erkannt und eliminiert.
Krebstherapien, die das Immunsystem einbeziehen, werden seit vielen Jahren in Form der allogenen Stammzelltransplantation bei AML-Patienten in bestimmten Erkrankungssituationen erfolgreich angewendet. In den letzten Jahren sind weitere neuartige immuntherapeutische Ansätze entwickelt worden, die derzeit klinisch geprüft werden. „Unsere Ergebnisse zeigen, wie die Krebsstammzellen das Immunsystem raffiniert austricksen. Die Aufklärung des dahinterstehenden Mechanismus ermöglicht es nun, zum Gegenschlag auszuholen“, sagt Andreas Trumpp, Deutsches Krebsforschungszentrum und HI-STEM.
Aus den Ergebnissen leitet sich die Möglichkeit ab, bösartige Leukämiestammzellen durch die Kombination von PARP-Inhibitoren mit aktiven NK-Zellen zu bekämpfen: Diesen Ansatz planen die beteiligten Wissenschaftler nun in einer klinischen Studie zu evaluieren.
An der nun in der Zeitschrift „Nature“ veröffentlichten Arbeit waren federführend beteiligt: Claudia Lengerke (Departement Biomedizin und Klinik für Hämatologie an der Universität und am Universitätsspital Basel), Helmut Salih (Universität Tübingen und Deutsches Krebskonsortium (DKTK) und Andreas Trumpp (Deutsches Krebsforschungszentrum, HI-STEM und DKTK).
*Das Heidelberg Institute for Stem Cell Technology and Experimental Medicine (HI-STEM) gGmbH wurde 2008 als Public-Private-Partnership vom DKFZ und der Dietmar Hopp Stiftung gegründet.
Anna M. Paczulla, Kathrin Rothfelder, Simon Raffel, Martina Konantz, Julia Steinbacher, Hui Wang, Claudia Tandler, Marcelle Mbarga, Thorsten Schaefer, Mattia Falcone, Eva Nievergall, Daniela Dörfel, Pauline Hanns, Jakob R. Passweg, Christoph Lutz, Juerg Schwaller, Robert Zeiser, Bruce R. Blazar, Michael A. Caligiuri, Stephan Dirnhofer, Pontus Lundberg, Lothar Kanz, Leticia Quintanilla-Martinez, Alexander Steinle, Andreas Trumpp, Helmut R. Salih, Claudia Lengerke: Absence of NKG2D ligands defines leukaemia stem cells and mediates their immune evasion.
Nature 2019, DOI: 10.1038/s41586-019-1410-1
Ein Bild steht zum Download zur Verfügung unter: nk-v2-quer.jpg
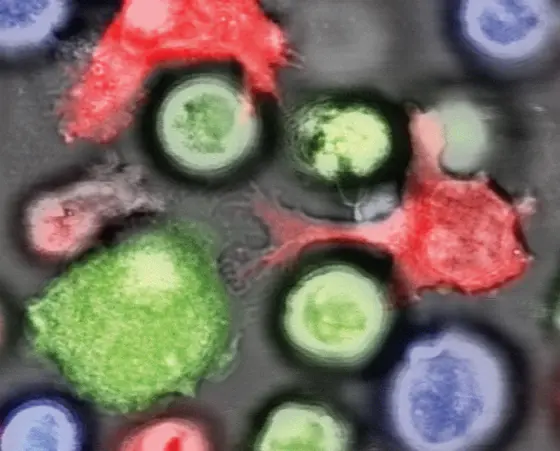
BU: Natürliche Killerzellen (rot) greifen gewöhnliche Leukämiezellen (grün) an. Leukämie-Stammzellen (blau) dagegen unterdrücken das Erkennungsmerkmal NKG2DL auf ihrer Oberfläche und entgehen so dem Immunangriff.
Nutzungshinweis für Bildmaterial zu Pressemitteilungen
Die Nutzung ist kostenlos. Das Deutsche Krebsforschungszentrum (DKFZ) gestattet die einmalige Verwendung in Zusammenhang mit der Berichterstattung über das Thema der Pressemitteilung bzw. über das DKFZ allgemein. Bitte geben Sie als Bildnachweis an: „Quelle: Schürch/Lengerke, Universität und Universitätsspital Basel“. Eine Weitergabe des Bildmaterials an Dritte ist nur nach vorheriger Rücksprache mit der DKFZ-Pressestelle (Tel. 06221 42 2854, E-Mail: presse@dkfz.de) gestattet. Eine Nutzung zu kommerziellen Zwecken ist untersagt.
Letzte Änderung: 18.07.2019