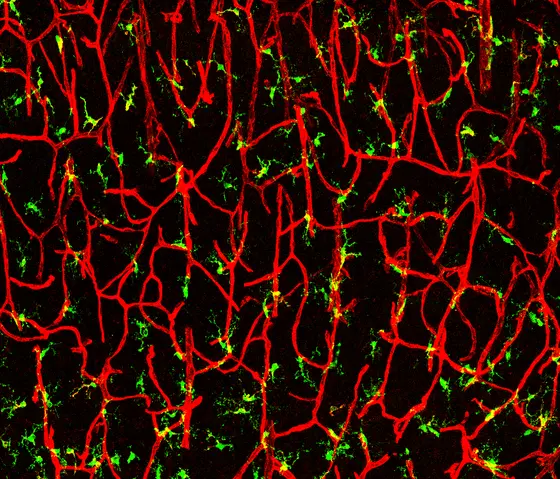
Wenn sich in einem Embryo das Zentralnervensystem (ZNS) entwickelt, entstehen nicht nur Nervenzellen und die Stützzellen des Nervensystems, sondern auch Blutgefäße. Diese versorgen das sich entwickelnde Gehirn mit Sauerstoff und Nährstoffen. Sowohl das Nerven- als auch das Blutgefäßsystem bilden verzweigte Netzwerke. Auch Riesenfresszellen (Makrophagen), die Immunzellen des ZNS, wandern in das sich entwickelnde Gehirn des Embryos ein.
Si Chen vom Team um Ana Martin-Villalba, Deutsches Krebsforschungszentrum (DKFZ) Heidelberg, zeigte nun, dass diese Immunzellen eine wichtige Rolle bei der Gehirnentwicklung spielen: „Wir haben in unserer aktuellen Arbeit gezeigt, dass das Immunsystem während der ZNS-Entwicklung mit dem Gefäß- und Nervensystem interagiert“, sagt die Wissenschaftlerin. Die ZNS-Makrophagen bilden das Signalmolekül CD95L, mit dem sie das gemeinsame Wachstum von Nervenzellen und Blutgefäßen steuern.
CD95L ist der Bindungspartner für den CD95-Rezeptor. Dieser Rezeptor wurde ursprünglich auf Lymphozyten entdeckt – dort löst er den programmierten Zelltod (Apoptose) aus, wenn er an seinen Bindungspartner, also CD95L, angedockt hat. Die Forschergruppe von Martin-Villalba hat in den vergangenen Jahren bereits zahlreiche weitere Funktionen von CD95 entdeckt. Die Forscher haben den Rezeptor auf vielen Zelltypen gefunden, z.B. auf Nerven-, Immun- und Tumorzellen. So spielt CD95 beispielsweise eine Rolle bei der Ausbreitung mancher Tumoren oder bei Entzündungen, erklärt Martin-Villalba.
Ihre neuen Ergebnisse zeigen nun, dass verschiedene Zelltypen im sich entwickelnden Gehirn CD95 bilden – und zwar in immer größerer Zahl im Lauf der Entwicklung. CD95L wird dagegen vor allem von Makrophagen gebildet: „Wir haben ZNS-Makrophagen als die Hauptquelle von CD95L identifiziert“, sagt Ana Martin-Villalba. „Durch die verzweigte Zellform der Makrophagen kommen sie in engen Kontakt mit den Blutgefäßen und Nervenfortsätzen. Daher spielen wahrscheinlich Zell-Zell-Wechselwirkungen eine wichtige Rolle – CD95L auf der Zelloberfläche der Makrophagen bindet an den CD95-Rezeptoren auf Nerven und Blutgefäßen.“ So steuern die ZNS-Makrophagen die koordinierte Entwicklung beider Systeme (Nerven und Blutgefäße) – „über das gleiche Molekül, nämlich CD95L, gemeinsam und gleichzeitig“, ergänzt die Wissenschaftlerin.
Das von Makrophagen gebildete CD95L aktiviert seinen passenden Rezeptor CD95 auf Blutgefäßen: Diese wachsen und verzweigen sich. Ebenso wird der Rezeptor CD95 auf Neuronen aktiviert: Die Nervenzellen verzweigen sich in der sich entwickelnden Hirnrinde und der Netzhaut des Auges.
In weiteren Versuchen untersuchte das Forscherteam von Martin-Villalba die Folgen, wenn zu wenig CD95-Rezeptoren bzw. zu wenig CD95-Liganden vorhanden sind: Dadurch wachsen die Blutgefäße und die Nervenzellen weniger, sie verzweigen sich weniger und die synaptische Aktivität der Neuronen ist geringer. „Es gibt Hinweise darauf, dass ein Fehlen von CD95 Verhaltensänderungen zur Folge haben kann. Mäuse, die wenig CD95-bilden, haben eine Reihe von Verhaltens- und kognitiven Defizite, sie sind z.B. ängstlicher und zeigen weniger spontane Aktivität“, erklärt Martin-Villalba. „Unsere Forschungsergebnisse unterstreichen die Bedeutung von Makrophagen für Entstehung des neurovaskulären Netzwerks während der Gehirnentwicklung.“
Auch in einen Tumor wandern viele Makrophagen ein. „Möglicherweise regen Makrophagen auch hier via CD95L Tumorzellen und Blutgefäße gemeinsam zum Wachstum an“, vermutet Martin-Villalba. „Das Signalmolekül könnte durch einen spezifischen Antikörper blockiert werden – und so das weitere Wachstum des Tumors und der Blutgefäße verhindern“, wagt Martin-Villalba einen Ausblick. Erste klinische Versuche mit einer Blockade der CD95-Aktivität als Zweittherapie bei Patienten mit Hirntumoren (Glioblastomen) seien vielversprechend verlaufen.
Si Chen, Nathalie Tisch, Marcel Kegel, Rosario Yerbes, Robert Hermann, Hannes Hudalla, Cecilia Zuliani, Gülce Sila Gülcüler, Klara Zwadlo, Jakob von Engelhardt, Carmen Ruiz de Almodóvar, Ana Martin-Villalba: Central nervous system macrophages control neurovascular development via CD95L. Cell Reports 2017, DOI: 10.1016/j.celrep.2017.04.056