Den potentiellen neuen Wirkstoff fanden die Wissenschaftler der Klinischen Kooperationseinheit des DKFZ und des Universitätsklinikums um Dr. Georg Gdynia und Professor Dr. Wilfried Roth, der jetzt am Universitätsklinikum Mainz tätig ist, in sogenannten Natürlichen Killerzellen. Stoßen diese bei ihren Patrouillen im Körper auf Tumorzellen, injizieren sie ihnen - vorausgesetzt, sie erkennen sie als solche - einen tödlichen Protein-Cocktail. Die Pathologen identifizierten in diesem Giftgemisch das sogenannte High Mobility Group Box 1 (HMGB1)-Protein als höchst effektive, natürliche Waffe gegen Krebs: Es legt einen Mechanismus der Energiegewinnung lahm, der in der Regel von Tumorzellen und nicht von gesunden Körperzellen genutzt wird. Diese Form des “Zellmordes“ durch das Immunsystem war bisher noch nicht bekannt. Gemeinsam mit Kollegen des Heidelberger Instituts für Theoretische Studien (HITS) und des Anorganisch-Chemischen Instituts der Universität Heidelberg haben die Wissenschaftler ihre Ergebnisse nun erstmals in der Fachzeitschrift Nature Communications beschrieben.
Die Killerzellen tragen das Proteingemisch, das Tumorzellen innerhalb weniger Minuten tötet, vorrätig in kleinen Bläschen (Granula) in sich. Diese Eigenschaft macht sie zu einem interessanten Objekt der Krebsforschung. Die Zusammensetzung des Gift-Cocktails ist daher bereits aufgeklärt. “Bisher wurden allerdings nur andere Wirkungen des Proteins HMGB1 beschrieben, z.B. dass es andere Immunzellen anlockt und sie ausreifen lässt“, erklärt Gdynia. “erst jetzt hat es sich als potentes Zellgift entpuppt.“
Tumoren im Tierversuch schrumpfen oder sterben teils vollständig ab
Nachdem es den Heidelberger Forschern gelungen war, das entscheidende Protein aus dem Gemisch herauszufiltern, zeigte sich in Versuchen mit Tumorzellen, dass es deutlich mehr kann als nur die Immunantwort zu verstärken: Es unterbricht einen wichtigen Stoffwechselweg, über den Tumorzellen den Zucker Glucose abbauen und so Energie gewinnen. Sämtliche molekularen Prozesse der Zellen kommen zum Erliegen. Um die Wirkung auf komplette Tumoren zu testen, stellte die Arbeitsgruppe größere Mengen des HMGB1-Proteins her: Sie regten Killerzellen von gesunden Blutspendern zur Freisetzung des Proteins an. In den mit HMGB1 behandelten Mäusen schrumpften angewachsene Dickdarmtumoren oder verschwanden sogar ganz.
“Immuntherapien zielen in der Regel darauf ab, das Immunsystem darin zu unterstützen, die Krebszellen besser zu erkennen und zu bekämpfen. Eine Therapie mit HMGB1 hätte den Vorteil, dass sie zwar die Waffen des Immunsystems nutzt, aber nicht von dessen Funktionsfähigkeit abhängt und trotzdem sehr selektiv gegen Krebszellen wirkt“, so Gdynia. Die Gewinnung des Proteins ist sehr diffizil, denn man muss das richtige erwischen: “Die Wirkung von HMGB1 war bisher so wenig greifbar, weil es unzählige verschiedene Varianten gibt, die sich zwar nur minimal unterscheiden, aber trotzdem andere Aufgaben erfüllen“, so der Pathologe. Nur HMGB1 aus den Granula der Killerzellen kann Tumoren töten, HMGB1 aus dem Kern der Zellen nicht. Auch mit Hilfe von Bakterien erzeugtes menschliches HMGB1 erzielt nicht dieselbe starke Wirkung. Die Arbeitsgruppe meldete das für ihre Forschung entwickelte Verfahren zur Gewinnung des Proteins aus Killerzellen sowie das neue Therapiekonzept zum Patent an. Ziel ist es, eine neue Therapieform für Krebspatienten zu entwickeln.
Für seine Entdeckung ist Dr. Georg Gdynia von der Deutschen Gesellschaft für Pathologie (DGP) bei ihrer 100. Jahrestagung in Berlin im Mai 2016 mit dem Novartis-Preis ausgezeichnet worden. Gdynia teilt sich den von der Firma Novartis Oncology gestifteten und mit 10.000 Euro dotierten Preis zu gleichen Teilen mit dem Biochemiker Dr. Jan Pencik von der Medizinischen Universität Wien.
Inzwischen haben Gdynia und seine Kollegen um Dr. Adelheid Cerwenka vom Deutschen Krebsforschungszentrum weitere Forschungsergebnisse im Journal “Molecular & Cellular Oncology“ veröffentlicht. Darin berichten die Wissenschaftler, dass HMGB1 auch besonders aggressive Krebszellen, die resistent gegen Bestrahlung und Chemotherapien sind, abtöten kann. Diese Tumorzellen sind meist nur schlecht an die Blutversorgung angebunden, benötigen für ihr Überleben kaum Sauerstoff und kommen mit widrigsten Lebensbedingungen zurecht. Derzeit entwickelt die Arbeitsgruppe den weltweit ersten Test, mit dem Onkologen in Zukunft prüfen können, wie hoch der Anteil dieser hochaggressiven Zellen im Tumor eines Patienten ist. Anhand dieser Information kann der Arzt genauer abschätzen, wie wahrscheinlich der Krebs nach einer Operation erneut heranwächst oder auf die gängigen Medikamente anspricht, und frühzeitig eine geeignetere Therapie auswählen. Mit diesem Test, dem sogenannte “Energetic Fingerprinting“ (EnFin), ist, im Rahmen des “eXist-Forschungstransfer“ des Bundesministeriums für Wirtschaft und Energie mit rund 700.000 Euro gefördert, eine Unternehmensgründung für 2017 geplant.
Ein Bild zur Pressemitteilung steht unter folgendem link zum Download zur Verfügung:
http://www.dkfz.de/de/presse/pressemitteilungen/2016/bilder/HMGB1.jpg
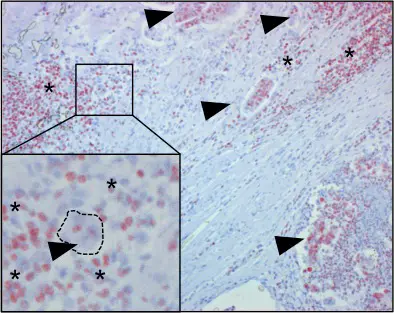
BU: HMGB1 positive (rote Färbung) Immunzellen infiltrieren einen Dickdarmtumor.
Ein Bild von Dr. Georg Gdynia steht unter folgendem link zum Download zur Verfügung:
http://www.dkfz.de/de/presse/pressemitteilungen/2016/bilder/gdynia.jpg
BU: Dr. Georg Gdynia, Klinische Kooperationseinheit für Molekulare Tumorpathologie des DKFZ und des Universitätsklinikums Heidelberg; Foto: Universitätsklinikum Heidelberg
Literatur:
Gdynia G, Sauer SW, Kopitz J, Fuchs D, Duglova K, Ruppert T, Miller M, Pahl J, Cerwenka A, Enders M, Mairbäurl H, Kaminski MM, Penzel R, Zhang C, Fuller JC, Wade RC, Benner A, Chang-Claude J, Brenner H, Hoffmeister M, Zentgraf H,Schirmacher P, Roth W. The HMGB1 protein induces a metabolic type of tumour cell death by blocking aerobic respiration. Nat Commun. 2016 Mar 7;7:10764. doi:10.1038/ncomms10764. PubMed PMID: 26948869; PubMed Central PMCID: PMC4786644.
Adelheid Cerwenka , Jürgen Kopitz , Peter Schirmacher , Wilfried Roth , Georg Gdynia.
HMGB1: the metabolic weapon in the arsenal of NK cells. Molecular & Cellular Oncology. http://dx.doi.org/10.1080/23723556.2016.1175538