Angewandte Bioinformatik
- DKTK
- Funktionelle und Strukturelle Genomforschung

Prof. Dr. Benedikt Brors
Wir kombinieren Methoden aus der Informatik, Bioinformatik und Statistik, um die Krebsentwicklung besser zu verstehen und die Diagnose und Therapie von Krebserkrankungen zu verbessern. Mit den Ergebnissen unserer bioinformatischen Analysen wollen wir klinische Anwendungen entwickeln, die langfristig Fortschritte bei der Versorgung und den Behandlungsmöglichkeiten von Krebspatienten ermöglichen.
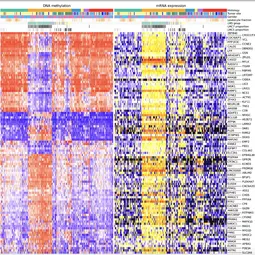
Unsere Forschung
Wir sind eine bioinformatische Abteilung, die sich mit der Analyse von hochdimensionalen Daten aus Krebserkrankungen durch moderne Computerverfahren beschäftigt. Die meisten dieser Daten stammen aus Hochdurchsatzsequenzierung, wie z. B. Ganzgenomsequenzierung, RNA-Sequenzierung, Bisulfit-Sequenzierung, ATAC-Sequenzierung sowie deren Varianten, mit denen man jede einzelne Zelle analysieren kann. Durch die Analyse dieser Daten erhalten wir einzigartige Einblicke in die Krebsmechanismen, die Entwicklung, das Fortschreiten, das Ansprechen auf die Therapie von Tumoren und ihrer Interaktionen mit dem Immunsystem. Dies hilft bei der Ermittlung optimaler, gezielter Therapien für jeden einzelnen Patienten („Personalisierte Onkologie“ oder „Präzisionsonkologie“).
Wir entwickeln Methoden und Arbeitsabläufe, die mit riesigen Datenmengen auf verteilten Rechensystemen umgehen und beziehen dabei Verfahren der künstlichen Intelligenz mit ein. Unsere Arbeitsabläufe wurden in klinische Studien des Nationalen Zentrums für Tumorerkrankungen implementiert. Darüber hinaus tragen wir zu klinischen Studien der European Study Group for Pancreatic Cancer und der Deutschen Neuroblastom-Studiengruppe bei.
Wir sind Teil des Nationalen Centrums für Tumorerkrankungen (NCT) und des Deutschen Konsortiums für translationale Krebsforschung (DKTK). Darüber hinaus tragen wir zu Infrastrukturen bei, z.B. dem Deutschen Netzwerk für Bioinformatik-Infrastruktur (de.NBI) und dem Deutschen Humangenom-Phänom-Archiv (GHGA).
Projekte
The Comparative Cancer Genomics team lead by Dr. Lars Feuerbach focuses on integrating sequencing and array data across tumor subtypes and patient cohorts. In these Pan-Cancer studies the similarities and differences in the interplay of epigenome, genome and transcriptome during carciogenesis are investigated in context of three main interests:
Focus 1 - Replicative Immortality and telomere biology in cancer
Focus 2 - Identification of regulatory cancer driver mutations for precision oncology applications
Focus 3 - Software tool development for the analysis of cancer cohorts
Furthermore, following up on the ICGC Early-onset Prostate Cancer consortium, we study prostate cancer as part of the Pan Prostate Cancer group of the ICGC ARGO project.
Our methodological expertise for computational cancer genome analysis comprises algorithm development, specialized datastructures for multi-omics data integration, data mining by machine learning, compact visualization of complex information, and statistical modeling.
The Tumor Heterogeneity and Evolution team lead by Dr. Sadaf Mughal focuses on the application of computational methods to analyze omics data from patient cohorts to understand cancer heterogeneity, tumor evolution and to decipher the immune crosstalk in cancer progression and metastatic spread. We are particularly interested in learning drug resistance mechanisms tumor employ during evolution. For this we are investigating longitudinal samples to predict the evolutionary trajectories of aggressive metastatic subclones. Furthermore, we are studying the tumor-immune coevolution to address inter- and intra-tumoural heterogeneity, dictating progression of disease.
The Computational Oncoimmunology team lead by Charles Imbusch focuses on questions regarding the immune system in general and more specifically under pathogenic conditions such as cancer. To address these questions NGS, as well as array technologies, are routinely utilized.
With the advent of multiple single cell technologies it is now possible to differentiate subpopulations captured in an assay, allowing to address cell heterogeneity and the discovery of rare cell populations. We focus on the downstream analysis of scRNA-seq and scTCR to robustly identify and describe cell populations, study dynamic cross-talk between tumor and immune cells while keeping up to date with most recent algorithmic developments.
Alternatively to single cell assays we apply and develop methods to deconvolute from bulk data cell types, integrating epigenetic and transcriptomic data to describe the tumor microenvironment.
The AI in Translational Cancer Research team led by Benedikt Brors develops predictive and prognostic models to guide therapy for cancer patients. We are currently contributing AI models to two clinical trials, ESPAC-6 for adjuvant treatment in resectable pancreatic cancer (phase III, sponsor: University Hospital Heidelberg), and NB2015-LR for low- and medium-risk neuroblastoma (phase III, sponsor: University Hospital Cologne).
Team
- Profil anzeigen

Prof. Dr. Benedikt Brors
Leiter der Abteilung
-
Dr. Lars Feuerbach
Teamleiter Comparative Cancer Genomics
-
Dr. Sadaf Shabbir Mughal
Teamleiterin Tumor Heterogeneity and Evolution
-
Dr. Charles Vomfelde genannt Imbusch
Teamleiter Computational Oncoimmunology
-
Dr. Oscar Gonzalez Velasco
Postdoktorand
-

Dr. Siao-Han Wong
Postdoktorandin
-
Dr. Evgeniya Denisova
Postdoktorandin
-
Karina Martinez
Doktorandin
-
Julia Münch
Doktorandin
-
Ferdinand Popp
Doktorand
-
Silja Schlue
Doktorandin
-
Prof. Dr. Ezekiel Femi Adebiyi
Gastwissenschaftler
-
Corinna Sprengart
Sekretariat
-
Hans Bartelmeß
Systemadministration
Ausgewählte Publikationen
Comprehensive Genomic and Transcriptomic Analysis for Guiding Therapeutic Decisions in Patients with Rare Cancers
Horak P, Heining C, Kreutzfeldt S, Hutter B, Mock A, Hüllein J, Fröhlich M, Uhrig S, (…),Brors B, Stenzinger A, Schröck E, Hübschmann D, Weichert W, Glimm H, Fröhling S
Single-cell chromatin accessibility landscape identifies tissue repair program in human regulatory T cells
Delacher M, Simon M, Sanderink L, (…), Brors B, Imbusch CD, Feuerer M
Pan-cancer analysis of whole genomes
ICGC/TCGA Pan-Cancer Analysis of Whole Genomes Consortium
Genomic footprints of activated telomere maintenance mechanisms in cancer
Sieverling L, Hong C, Koser SD, Ginsbach P, Kleinheinz K, Hutter B, (…), PCAWG-Structural Variation Working Group; Brors B, Rippe K, Jones DTW, Feuerbach L; PCAWG Consortium
Kontaktieren Sie uns

