Medulloblastome sind seltene bösartige Tumoren des Kleinhirns, die vorwiegend bei Kindern vorkommen. Wissenschaftler gehen davon aus, dass in vielen Fällen erbliche Gendefekte die Entstehung dieser bösartigen Krebserkrankung auslösen. Standards für ein Routinescreening der Patienten nach solchen bekannten genetischen Faktoren oder gar Richtlinien und eine entsprechende flächendeckende Infrastruktur für die genetische Beratung betroffener Familien gibt es bisher allerdings nicht.
Nun ist es Wissenschaftlern gelungen, das Erbgut von 1022 Medulloblastom-Patienten genauer zu charakterisieren und daraus eine Empfehlung für das genetische Patientenscreening abzuleiten. „Wir haben so genannte Prädispositionsgene analysiert, also Gene, die mit der Entwicklung unterschiedlichster Krebsarten bei Kindern und Erwachsenen in Zusammenhang gebracht werden“, sagt Sebastian Waszak vom EMBL Heidelberg, einer der Erstautoren der Studie. Es stellte sich heraus, dass sechs dieser Gene bei Medulloblastom-Patienten deutlich häufiger als erwartet von einer genetischen Veränderung betroffen waren.
Analysierte man diese sechs Gene statistisch, so zeigte sich, dass bei etwa fünf Prozent der untersuchten Patienten das Krebsrisiko erhöht war. Berücksichtigte man alle Krebsrisiko-Gene bei der Auswertung, so hatten elf Prozent der Patienten ein erhöhtes Krebsrisiko. Betrachtete man eine spezielle Untergruppe allein, die so genannten „SHH-Medulloblastome“, so betrug der Anteil sogar 20 Prozent.
Mutationen in Prädispositionsgenen kommen in jeder einzelnen Zelle des Patienten vor und werden auch an die Nachkommen weitervererbt. „Mutationen dieser Art deuten häufig auf eine familiäre Veranlagung für Krebserkrankungen hin und stellen deshalb besondere Anforderungen an die Behandlung der Patienten und die Beratung der Familien“, erklärt Paul Northcott vom St. Jude Children's Research Hospital in Memphis, der sich die Erstautorenschaft mit Waszak teilt. Mehr Gewicht bekommen die Ergebnisse dadurch, dass nicht nur Material aus früheren Untersuchungen, sondern auch Patientendaten aus vier laufenden oder kürzlich abgeschlossenen klinischen Studien in die Analysen einbezogen wurden.
Basierend auf diesen Erkenntnissen sowie weiteren Tumormerkmalen entwickelten die Wissenschaftler Kriterien für ein genetisches Routine-Screening. „Erbliche Krankheitsfaktoren haben meist erheblichen Einfluss auf die ganze Familie des Patienten“, sagt Stefan Pfister, KiTZ Direktor, Wissenschaftler am Deutschen Krebsforschungszentrum sowie Oberarzt am Universitätsklinikum Heidelberg. „Wir möchten erreichen, dass die genetische Analyse bei Patienten mit bestimmten Formen des Medulloblastoms als Standard-of-care-Verfahren angeboten wird.“ Um dies flächendeckend zu ermöglichen, hat Pfister vor kurzem zusammen mit Christian Kratz von der Medizinischen Hochschule Hannover ein Register für Patienten mit erblicher Krebsprädisposition ins Leben gerufen. Außerdem haben sie eine Website erstellt, die viele nützliche Informationen für Patienten, Familien und Ärzte enthält: www.krebs-praedisposition.de.
Das Projekt wurde maßgeblich unterstützt vom Deutschen Krebskonsortium (DKTK), der Deutschen Krebshilfe, der Deutschen Kinderkrebsstiftung und dem Bundesministerium für Bildung und Forschung (BMBF).
Originalpublikation:
Waszak et al. Spectrum and prevalence of genetic predisposition in medulloblastoma: a retrospective genetic study and prospective validation in a clinical trial cohort. The Lancet Oncology. Online publication 10. Mai 2018; DOI: dx.doi.org/10.1016/S1470-2045(18)30242-0
Ein Bild zur Pressemitteilung steht zum Download zur Verfügung:
Medulloblastom-MRT-Hellerhoff-Wikimedia.jpg
Bildunterschrift:
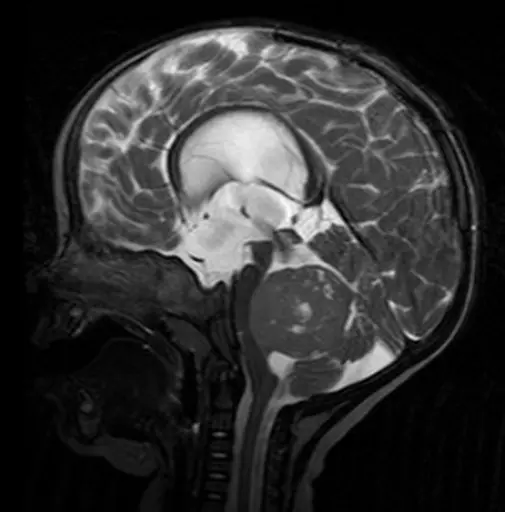
MRT-Aufnahme eines Medulloblastoms
Nutzungshinweis für Bildmaterial zu Pressemitteilungen
Die Nutzung ist kostenlos. Das Deutsche Krebsforschungszentrum (DKFZ) gestattet die einmalige Verwendung in Zusammenhang mit der Berichterstattung über das Thema der Pressemitteilung bzw. über das DKFZ allgemein. Bitte geben Sie als Bildnachweis an: „Quelle: Wikimedia/Hellerhoff“.
Eine Weitergabe des Bildmaterials an Dritte ist nur nach vorheriger Rücksprache mit der DKFZ-Pressestelle (Tel. 06221 42 2854, E-Mail: presse@dkfz.de) gestattet. Eine Nutzung zu kommerziellen Zwecken ist untersagt.